Oxford y Astrazeneca repetirán el ensayo de la vacuna por las dudas sobre la eficacia
La Universidad de Oxford y Astrazeneca realizarán una prueba más para aclarar la incertidumbre que se ha generado en torno a la eficacia de su vacuna
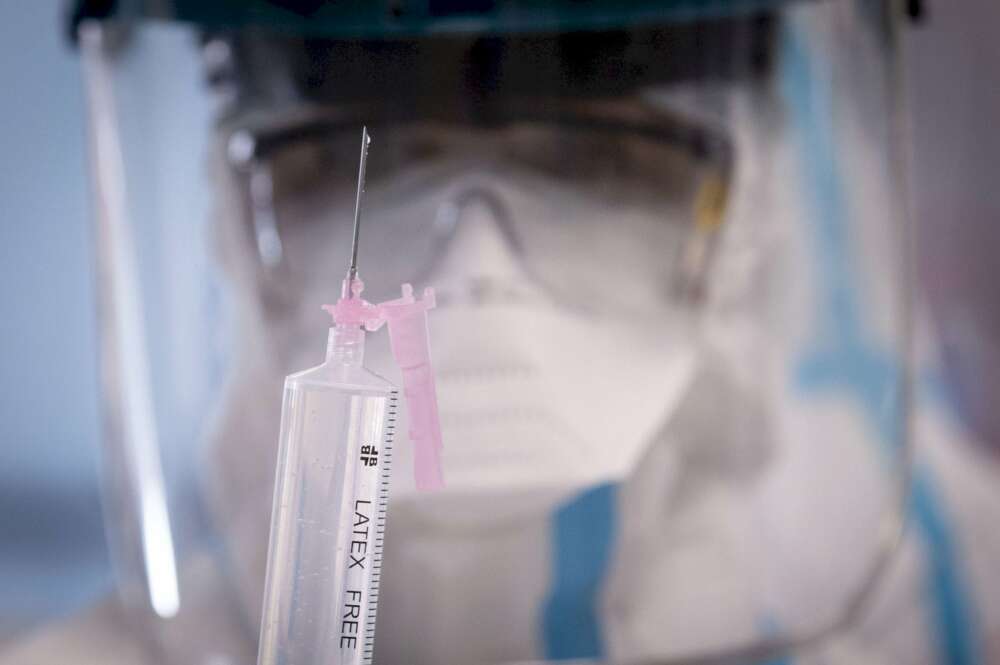
La vacuna de Oxford y Astrazeneca da un paso atrás. Los fabricantes tendrán que realizar un nuevo ensayo clínico a nivel global para aclarar la incertidumbre que se ha generado en torno a la eficacia de este remedio contra el coronavirus. Este antídoto demostró ser eficaz en un 70%. Y tan solo unos días después de comunicar su rendimiento, las entidades británicas anunciaron una fórmula de aplicación podría aumentar su efectividad hasta el 90%. Esta estrategia no convenció a los expertos.
Este alto porcentaje se alcanzó mediante un error. Las entidades británicas descubrieron que una primera dosis fuerte podría rebajar la eficacia de la segunda. Es decir, dos dosis completas mostraron una eficacia del 62% mientras que media dosis y, posteriormente, una entera, alcanzaba ese 90%. Y este baile de porcentajes es lo que llevará de nuevo a Oxford y Astrazeneca a retomar las pruebas.
«Ahora que hemos encontrado lo que parece una mejor eficacia, tenemos que validar esto, por lo que necesitamos hacer un estudio adicional»
«Ahora que hemos encontrado lo que parece una mejor eficacia, tenemos que validar esto, por lo que necesitamos hacer un estudio adicional», explicó el director ejecutivo de Astrazeneca, Pascal Soriot, en una entrevista con Bloomberg. “Probablemente haremos otro «estudio internacional, pero este podría ser más rápido porque sabemos que la eficacia es alta, por lo que necesitamos un número menor de pacientes”, añadió.
El nuevo ensayo no retrasará la autorización de emergencia
Soriot aseguró que esta nueva prueba adicional no retrasará las aprobaciones regulatorias en el Reino Unido y la Unión Europea. El Gobierno de Boris Johnson pidió hace una semana al regulador de medicamentos la evaluación para autorizar de emergencia la vacuna. El Reino Unido aprobó una ley por la que puede aprobar uno de los prototipos ante de que lo haga el regulador europeo. Pero solo tiene hasta enero para hacerlo.
En cambio, en los Estados Unidos la autorización se puede demorar. “Es poco probable que el regulador apruebe la vacuna sobre la base de estudios realizados en otros lugares, especialmente dadas las preguntas sobre los resultados”, señaló Soriot. “Aún se espera la autorización en algunos países antes de fin de año, agregó.
Científicos ponen en duda la vacuna
La críticas más severas a la investigación británica llegaron por parte del director del programa de vacunas estadounidense Operation Warp Speed, Moncef Slaoui, quien sentenció que el mayor nivel de efectividad se ha probado únicamente en la población joven.
A él se sumaron los ataques de los asesores del regulador de medicamentos estadounidense (FDA) y de los científicos de los Centros para el Control y la Prevención de Enfermedades (CDC). Ambos organismos han criticado que los fabricantes no han explicado cómo ha llegado a la conclusión de que su prototipo tiene un 70% de efectividad.
«Si no se sabe esto, es difícil saber la importancia de sus hallazgos», señaló, Paul Offit, miembro del Comité Asesor de Vacunas y Productos Biológicos Relacionados de la FDA, uno de los encargados de revisar las vacunas Covid-19 antes de que se comercialicen, en declaraciones a la CNN. Tanto Pfizer como Moderna publicaron los datos que las llevaron a concluir la eficacia de sus antídotos.
Las entidades estadounidenses, además, hicieron hincapié en la falta de transparencia generalizada en la investigación. Según el comunicado que emitió Astrazeneca este lunes, 23.000 personas formaron parte de su ensayo de fase 3. Como es habitual, algunos de los voluntarios recibieron la vacuna anticovid mientras que otros simplemente un placebo.
El laboratorio británico explicó que 131 participantes desarrollaron Covid-19. Sin embargo, no especifica cuántas personas recibieron la inyección correcta y cuántas no, lo que genera escepticismo. Ninguno de los portavoces