EE.UU. contra la vacuna de Oxford: “La alta eficacia solo funciona en los jóvenes”
El director de la Operation Warp Speed critica que Oxford y Astrazeneca han comprobado la efectividad de la fórmula de una dosis y media solo en los jóvenes
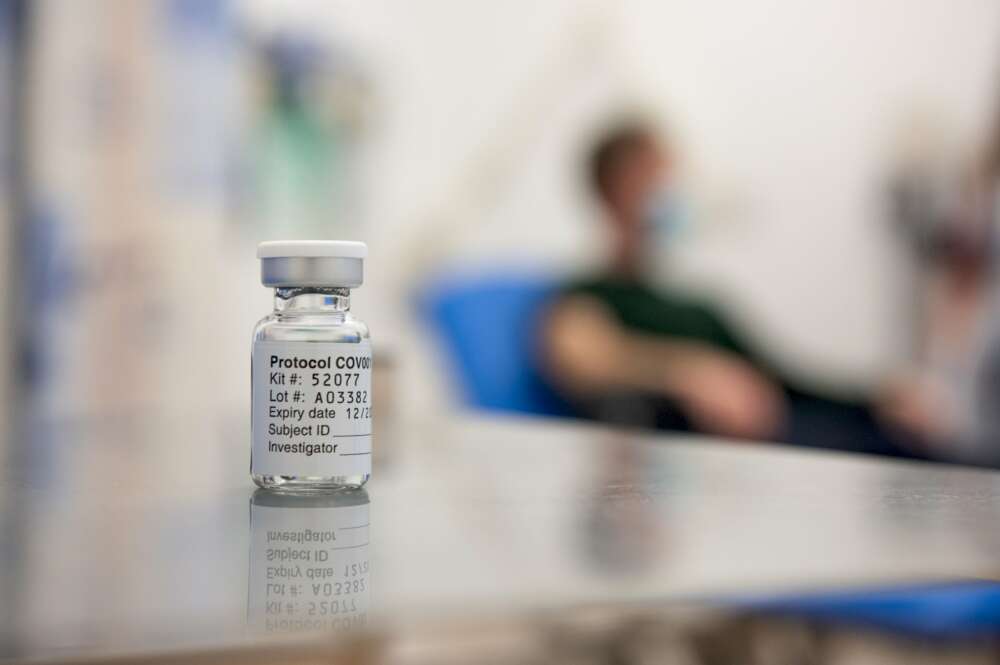
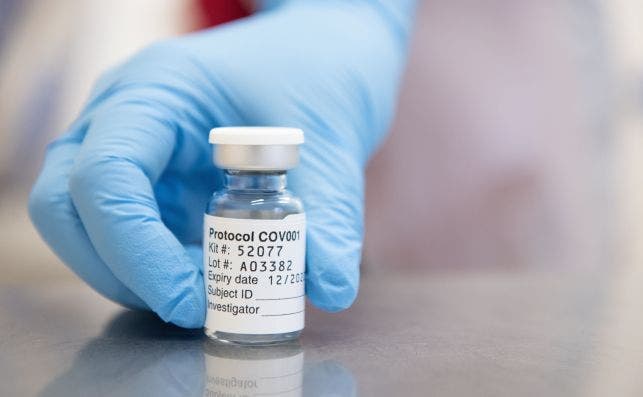
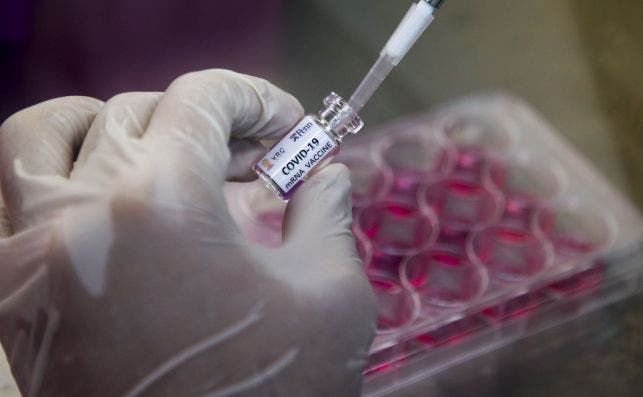
Los resultados preliminares de la vacuna de la Universidad de Oxford y Astrazeneca están dando de qué hablar. Este antídoto contra el coronavirus demostró ser eficaz ‘solo’ en un 70% – dentro de los estándares inmunidad homologables exigidos– frente a los de Moderna y Pfizer, que superan el 95%. Pero tan solo unos días después de comunicar su rendimiento, las entidades británicas anunciaron una fórmula de aplicación podría aumentar su efectividad hasta el 90%. Y esta estrategia no ha convencido a los expertos de los Estados Unidos.
Los fabricantes de la vacuna británica descubrieron que una primera dosis fuerte podría rebajar la eficacia de la segunda. Es decir, dos dosis completas mostraron una eficacia del 62% mientras que media dosis y, posteriormente, una entera, alcanzaba ese 90%. Uno de los principales investigadores de Oxford, Adrian Hill, explicó que «probablemente se necesitarían semanas y meses» para comprender por qué la dosis más baja producía resultados mucho mejores.
Esta explicación de la Universidad de Oxford no gustó al director del programa de vacunas estadounidense Operation Warp Speed, Moncef Slaoui, quien ha sentenciado que el mayor nivel de efectividad se ha probado únicamente en la población joven, según ha adelantado Bloomberg.
Analistas y expertos ponen en duda la vacuna de Oxford y Astrazeneca
En un comunicado, Oxford dijo que, tras hablar con los reguladores de medicamentos, llegaron a un acuerdo para seguir adelante con los dos regímenes. “Los métodos para medir la concentración ya están establecidos y podemos asegurar que todos los lotes de vacuna ahora sean equivalentes”, aseguró la universidad.
Pero si ya existían dudas sobre esta vacuna, la acusación de Slaoui no ha hecho más que aumentar el escepticismo de los expertos. «La explicación más probable de la eficacia divergente en su análisis intermedio es el azar o la demografía del paciente», criticó Sam Fazeli, analista de Bloomberg Intelligence, en una nota.
«Los métodos para medir la concentración ya están establecidos y podemos asegurar que todos los lotes de vacuna ahora sean equivalentes»
«De cualquier manera, la aprobación basada en datos actuales significa que las personas serán inoculadas con una vacuna cuya verdadera eficacia se desconoce», añadió.
Saad Omer, especialista en vacunas de la Facultad de Medicina de Yale, también atacó la investigación. Este experto señaló que el grupo con la tasa de eficacia del 90% era relativamente pequeño, por lo que era posible que esos resultados no sean los mismos en grupos más grandes.
Y es que para Omer, existe una falta de claridad en varios aspectos de la vacuna de Oxford y Astrazeneca. «Odio criticar a mis compañeros académicos, o cualquier otra persona, pero divulgar información como esta es como pedirnos que intentemos leer las hojas de té», concluyó.
La FDA y los CDC reclaman mayor transparencia de la vacuna británica
La vacuna de Oxford y Astrazeneca también ha recibido ataques de los asesores del regulador de medicamentos estadounidense (FDA) y de los científicos de los Centros para el Control y la Prevención de Enfermedades (CDC). Ambos organismos han criticado que los fabricantes no han explicado cómo ha llegado a la conclusión de que su prototipo tiene un 70% de efectividad.
«Si no se sabe esto, es difícil saber la importancia de sus hallazgos», señaló, Paul Offit, miembro del Comité Asesor de Vacunas y Productos Biológicos Relacionados de la FDA, uno de los encargados de revisar las vacunas Covid-19 antes de que se comercialicen, en declaraciones a la CNN. Tanto Pfizer como Moderna publicaron los datos que las llevaron a concluir la eficacia de sus antídotos.
Las entidades estadounidenses, además, hicieron hincapié en la falta de transparencia generalizada en la investigación. Según el comunicado que emitió Astrazeneca este lunes, 23.000 personas formaron parte de su ensayo de fase 3. Como es habitual, algunos de los voluntarios recibieron la vacuna anticovid mientras que otros simplemente un placebo.
El laboratorio británico explicó que 131 participantes desarrollaron Covid-19. Sin embargo, no especifica cuántas personas recibieron la inyección correcta y cuántas no, lo que genera escepticismo. Ninguno de los portavoces
Sin rastro de las reacciones adversas graves que paralizaron los ensayos
Y tampoco han dado explicaciones de los motivos por los que las pruebas llegaron a suspenderse hasta en dos ocasiones después de que dos participantes sufrieran reacciones adversas graves.
«Me gustaría conocer los datos específicamente sobre esas reacciones adversas graves que hicieron que el ensayo se detuviera»
«Me gustaría conocer los datos específicamente sobre esas reacciones adversas graves que hicieron que el ensayo se detuviera», indicó William Schaffner, miembro del Comité Asesor de Prácticas de Inmunización de los CDC, que también revisará las vacunas antes de que éstas salgan al mercado.
En el documento, Astrazeneca afirma que «no se han confirmado eventos de seguridad graves relacionados con la vacuna» y que la vacuna fue «bien tolerada». Sin embargo, todavía no han dado explicaciones de qué ocurrió cuando la investigación se paralizó.