Los expertos ponen en duda la vacuna de Oxford y Astrazeneca
Estos son los puntos de la vacuna de Oxford y Astrazeneca que critican los científicos: desde falta de transparencia hasta dudas sobre su seguridad
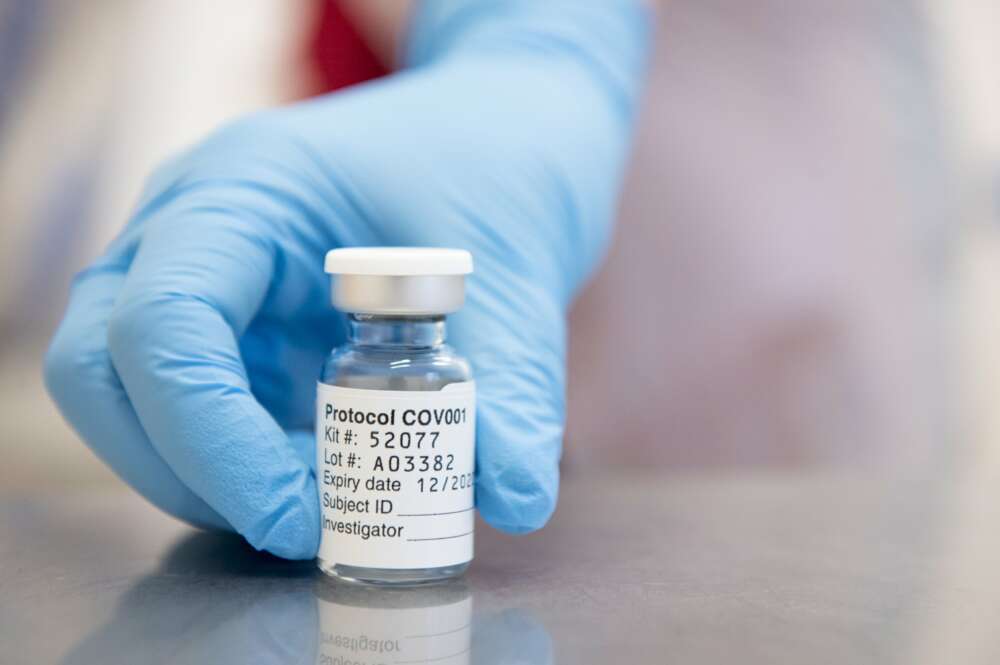
Una dosis de la vacuna de Covid-19 de la Universidad de Oxford y Astrazeneca, que descubrieron una mayor protección en pacientes de los ensayos clínicos que recibieron dosis menores | EFE/EPA/Oxford/JC
Los datos que la Universidad de Oxford y Astrazeneca han aportado sobre la tercera y última etapa del ensayo clínico de la vacuna contra el coronavirus no son suficientes para los expertos. Asesores del regulador de medicamentos estadounidense (FDA) y científicos de los Centros para el Control y la Prevención de Enfermedades han criticado que ninguna de estas entidades ha explicado cómo ha llegado a la conclusión de que su prototipo tiene un 70% de efectividad.
«Si no se sabe esto, es difícil saber la importancia de sus hallazgos», ha explicado, Paul Offit, miembro del Comité Asesor de Vacunas y Productos Biológicos Relacionados de la FDA, uno de los encargados de revisar las vacunas Covid-19 antes de que se comercialicen, en declaraciones a la CNN. Tanto Pfizer como Moderna publicaron los datos que las llevaron a concluir la eficacia de sus antídotos.
Astrazeneca no especifica cuántos voluntarios recibieron la vacuna y cuántos placebo
Según el comunicado que emitió Astrazeneca este lunes, 23.000 personas formaron parte de su ensayo de fase 3. Como en todas las investigaciones, algunos de los voluntarios recibieron la vacuna anticovid mientras que otros simplemente un placebo.
El laboratorio británico explicó que 131 participantes desarrollaron Covid-19. Sin embargo, no especifica cuántas personas recibieron la inyección correcta y cuántas no, lo que genera escepticismo. Ninguno de los portavoces
Los expertos plantean dudas sobre la seguridad de la vacuna
Los expertos también tienen dudas sobre la seguridad de este remedio. Los ensayos clínicos llegaron a suspenderse hasta en dos ocasiones después de que dos participantes sufrieran reacciones adversas graves. No obstante, los reguladores permitieron continuar las investigaciones.
«Me gustaría conocer los datos específicamente sobre esas reacciones adversas graves que hicieron que el ensayo se detuviera»
«Me gustaría conocer los datos específicamente sobre esas reacciones adversas graves que hicieron que el ensayo se detuviera», ha indicado William Schaffner, miembro del Comité Asesor de Prácticas de Inmunización de los CDC, que también revisará las vacunas antes de que éstas salgan al mercado.
En el documento, Astrazeneca afirma que «no se han confirmado eventos de seguridad graves relacionados con la vacuna» y que la vacuna fue «bien tolerada». Sin embargo, todavía no han dado explicaciones de qué ocurrió cuando la investigación se paralizó.
Los científicos preguntan por la dosis
Entre los participantes del estudio que recibieron la vacuna Covid-19, hubo dos regímenes de dosis diferentes. Uno de ellos englobó a 2.741 participantes que recibieron media dosis de la vacuna y luego una dosis completa al menos un mes después. En el segundo grupo, a 8.895 participantes se les inyectó una dosis completa seguida de otra dos al menos un mes después.
El primer grupo, el de la media dosis, estaba protegido en un 90% contra el coronavirus, mientras que el segundo solo lo estaba en un 62%. Uno de los principales investigadores de Oxford, Adrian Hill, ha explicado que «probablemente se necesitarían semanas y meses» para comprender por qué la dosis más baja producía resultados mucho mejores.
«No entendemos completamente eso, pero hay varias ideas sobre cómo podría funcionar, y las estamos explorando», ha apuntado Hill este lunes en la CNN. En este sentido, Saad Omer, especialista en vacunas de la Facultad de Medicina de Yale, señaló que el grupo con la tasa de eficacia del 90% era relativamente pequeño, por lo que era posible que esos resultados no sean los mismos en grupos más grandes.
Para Omer, existe una falta de claridad en varios aspectos de la vacuna de Oxford y Astrazeneca. «Odio criticar a mis compañeros académicos, o cualquier otra persona, pero divulgar información como esta es como pedirnos que intentemos leer las hojas de té», concluyó.