La UE acelera la vacuna de Oxford y Astrazeneca
La Agencia Europea de Medicamentos iniciará una revisión del prototipo para acortar los tiempos de su lanzamiento
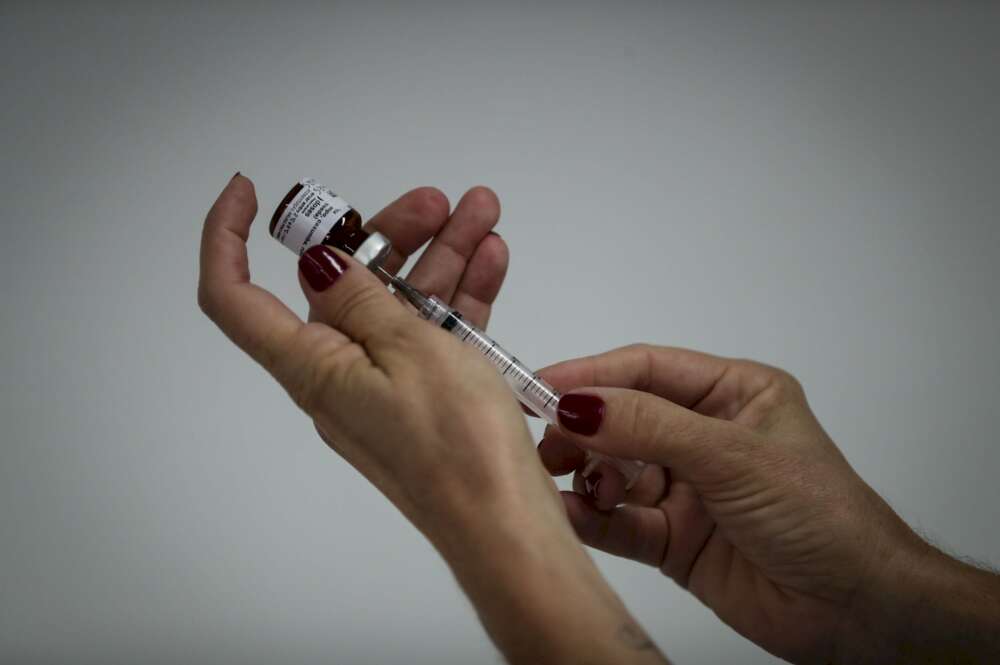
Europa está dispuesta a dar un paso adelante para dar luz cuanto antes a la vacuna contra el coronavirus que han diseñado la Universidad de Oxford y la farmacéutica Astrazeneca. Los reguladores europeos iniciarán en los próximos días una revisión acelerada del prototipo para acortar el tiempo necesario para su lanzamiento en el continente.
La Agencia Europea de Medicamentos pondrá en marcha a lo largo de la semana estas comprobaciones que son imprescindibles para aprobar cualquier medicamento de urgencia, según han informado fuentes de la organización a Bloomberg.
En un contexto habitual, los desarrolladores de vacunas o medicamentos envían datos de las pruebas a los reguladores para que lleven a cabo la revisión que puede prolongarse durante meses. Sin embargo, en casos de emergencia estos plazos pueden acortarse.
La decisión convierte a la vacuna británica en el candidato número uno en toda Europa para vencer al coronavirus. Ninguna farmacéutica ha logrado acceder a esta fase de la investigación, uno de los últimos requisitos para que se inicie la inmunización en los países miembro del bloque.
Europa tiene sus esperanzas puestas en la vacuna de Oxford
La Unión Europea ya demostró su confianza en el prototipo de Oxford cuando realizó la primera compra de 30 millones de dosis de la vacuna, que se distribuirán entre los países a final de año si concluyen con éxito todas las pruebas clínicas. Fue el primero de los contratos del bloque, que también se ha garantizado la adquisición de 300 millones de dosis del antígeno que ha desarrollado la farmacéutica Sanofi.
La decisión de la Agencia Europea de Medicamentos sirve para dar carpetazo a algunas de las dudas que ha generado la vacuna británica durante los ensayos clínicos. Hasta dos pacientes llegaron a desarrollar complicaciones de salud durante las pruebas con grupos de voluntarios humanos. Un problema que obligó temporalmente a suspender la investigación. Ambos desarrollaron síntomas de la mielitis transversa durante las pruebas, aunque los investigadores no lo achacaron a la vacunación.
Las autoridades británicas dieron su consentimiento para que los ensayos se reanudasen por lo que la Universidad de Oxford y Astrazeneca continuaron con sus pruebas masivas en Reino Unido, Sudáfrica, Brasil e India.





