La EMA estudia la autorización del uso de la vacuna de Moderna en niños de 6 y 11 años
La Agencia Mundial del Medicamento espera concluir la evaluación de los datos del estudio clínico en "aproximadamente" dos meses
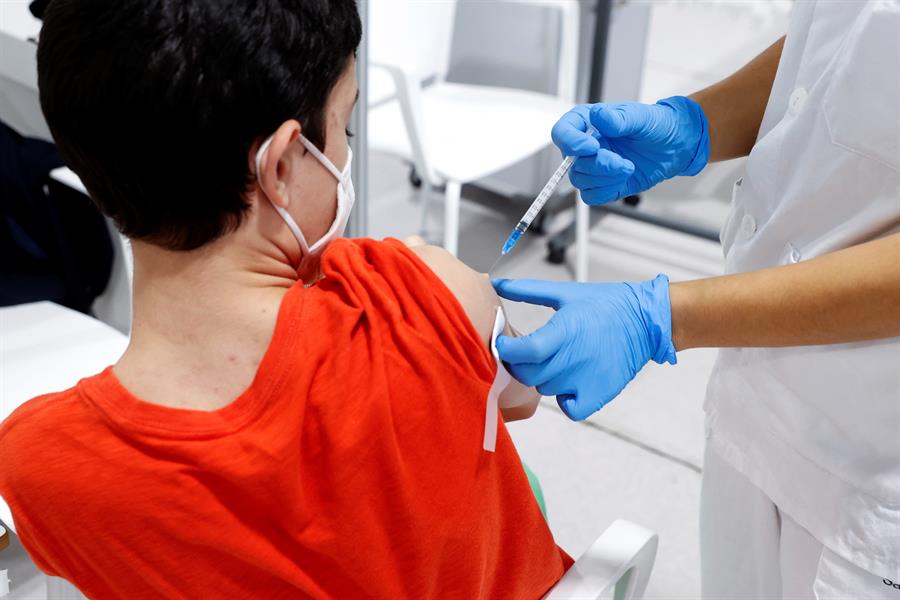
Un adolescente se vacuna en el hospital Enfermera Isabel Zendal de Madrid, este miércoles. Madrid se suma a las regiones que vacunan a mayores de 12 años. EFE/Chema Moya
La Agencia Europea del Medicamento (EMA, por sus siglas en inglés) ha anunciado este miércoles que ha empezado la evaluación del estudio clínico de uso de la vacuna de Moderna contra la Covid-19 en niños de entre 6 y 11 años, una vacuna que solo está autorizada, actualmente, para la población mayor de 12 años.
La EMA ha asegurado que prevé concluir con la evaluación de los dato del estudio en aproximadamente «dos meses». Aunque la agencia tiene en cuenta la posibilidad de que se necesite información o análisis complementarios, sin embargo, este es un calendario más corto en comparación con tipos similares de revisiones fuera de una pandemia.
No obstante, tras la conclusión de la agencia del medicamente, la Comisión Europea tendrá la última palabra sobre la extensión de la licencia de la vacuna de Moderna en los niños del rango de edad mencionado.
Moderna recibió su licencia europea para el uso de su vacuna del Covid-19 en adultos el pasado enero, lo que después se extendió a los adolescentes de más de 12 años en julio. Por su parte, el pasado mes de octubre, Moderna informó de datos provisionales positivos del estudio de fase 2/3 que estudia su vacuna contra la COVID-19 en niños de 6 a menos de 12 años de edad.
Este análisis provisional mostró una sólida respuesta de anticuerpos neutralizantes tras dos dosis de la vacuna en dosis de 50 ug, con un perfil de seguridad favorable.
Por el momento, las vacuna de ARNm de Pfizer/BioNtech y Moderna son los únicos dos preparados contra la covid-19 que se están utilizando en la actualidad en adolescentes mayores de 12 años en la Unión Europea (UE).
Tercera dosis de refuerzo en mayores de 69 años
Por otro lado, la Comisión de Salud Pública dió luz verde a principios de octubre a la administración de la tercera dosis de refuerzo de la vacuna de ARNm (Pfizer y Moderna) a los mayores de 69 años a partir del pasado 25 de octubre, una vez haya transcurrido los 6 meses desde la pauta inicial completa.
Una decisión que se tomó un día después de que la Agencia Europea del Medicamento autorizara la tercera dosis contra la Covid-19 para los mayores de 18 años a los seis meses de la segunda. Asimismo, la EMA avaló dar una nueva dosis de la vacuna a los pacientes inmunodeprimidos y a los residentes de los centros de mayores, algo que España ya está haciendo.






